Eine potenzielle neue Behandlung für das multiple Myelom
Melflufen (Melphalanflufenamid) ist ein neues Medikament, das zur Behandlung des rezidivierten oder refraktären multiplen Myeloms (RRMM) untersucht wird. Es ist ein Derivat des Chemotherapeutikums Melphalan. Melflufen ist ein Peptid-Wirkstoff-Konjugat; eine Kombination aus Melphalan und einem Peptid (kleines Protein), die miteinander verbunden sind. Melflufen wird als intravenöse Infusion (in die Vene) verabreicht.
Das Medikament wurde im Juli 2020 als neuer Arzneimittelantrag bei der US-amerikanischen Food and Drug Administration (FDA) eingereicht. Die FDA gewährte dem Antrag eine vorrangige Prüfung und eine Entscheidung wird für Ende Februar 2021 erwartet. Melflufen ist noch nicht allgemein verfügbar, da es für die Anwendung beim Myelom nicht zugelassen und zugelassen ist. Patienten können jedoch im Rahmen einer klinischen Studie mit dem Medikament behandelt werden.
:max_bytes(150000):strip_icc()/GettyImages-1279817557-a63a6fea0fb24167990a2062c52d43f0.jpg)
SimpleImages / Getty Images
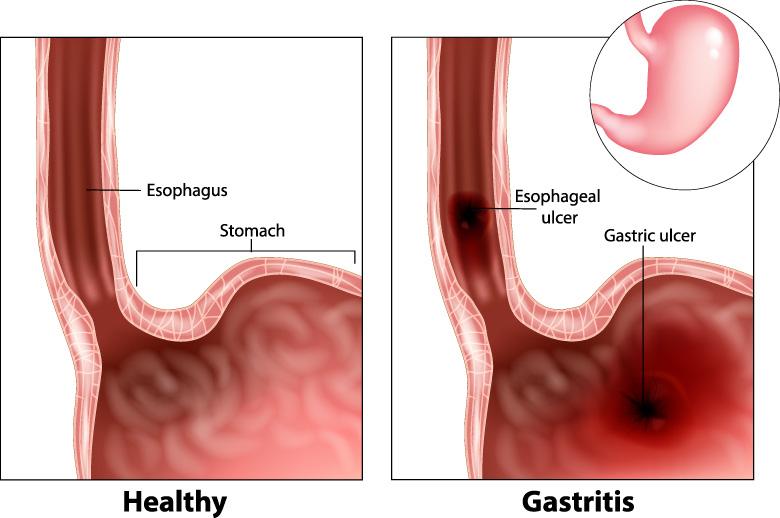
Was ist Multiples Myelom?
Das Multiple Myelom ist eine seltene, unheilbare Blutkrebsart, die auch als hämatologischer Krebs bekannt ist. Es betrifft Zellen, die Plasmazellen genannt werden, bei denen es sich um weiße Blutkörperchen handelt. Es gibt keine Heilung für das Multiple Myelom und es kehrt fast immer zurück, woraufhin man von einer „rezidivierten oder refraktären“ Krankheit spricht.
Wie funktioniert Melflufen?
Da neue Kombinationen von Antimyelom-Medikamenten in früheren Therapielinien eingeführt werden, haben Menschen mit RRMM häufig eine Krankheit, die gegen mehrere Medikamente resistent ist. Daher werden dringend Medikamente mit neuartigen Wirkmechanismen benötigt.
Melflufen hat in Kombination mit dem Steroid Dexamethason das Potenzial, diesen ungedeckten medizinischen Bedarf zu decken, indem es Folgendes bereitstellt:
- Ein neuartiger Wirkmechanismus
- Klinisch bedeutsame Wirksamkeit
- Überschaubare Sicherheit
Melflufen tötet Myelomzellen durch den Einsatz von Peptidasen (Enzyme, die Peptide abbauen) ab, die in Myelomzellen oft in höherer Zahl vorkommen als in gesunden Zellen. Wenn Melflufen in Myelomzellen eindringt, brechen die Peptidasen innerhalb der Zelle die Bindung, die das Melphalan und die Peptidase zusammenhält. Dadurch wird aktives Melphalan innerhalb der Myelomzelle freigesetzt. Das Melphalan verursacht dann irreversible DNA-Schäden, die zum Zelltod führen.
Was die Forschung sagt
Die Forschung ist im Gange, um neue Behandlungsmethoden für das multiple Myelom zu finden und Wege zu finden, die Anwendung bestehender zu verbessern.
Um die Forschung zu unterstützen, werden Sie möglicherweise gebeten, während Ihrer Behandlung an einer klinischen Studie teilzunehmen.
Melflufen wird derzeit in klinischen Studien zur Behandlung von RRMM-Patienten untersucht. Zu den klinischen Studien, in denen die Wirksamkeit von Melflufen untersucht wurde, gehören:
Die O-12-M1-Studie
O-12-M1 war eine internationale, multizentrische Phase-I/II-Studie zur Bestimmung der Dosis von Melflufen in Kombination mit Dexamethason und zur Untersuchung des Behandlungsansprechens bei Patienten mit RRMM, die gegenüber der letzten Therapielinie refraktär (resistent) waren.
In die O-12-M1-Studie wurde zwischen Juli 2013 und Dezember 2016 eine Gruppe von 45 Patienten eingeschlossen, die mindestens zwei vorangegangene Therapien erhalten hatten. Ziel der Studie war es, die maximal verträgliche Dosis von Melflufen zu ermitteln. Die etablierte maximal verträgliche Dosis betrug 40 mg Melflufen in Kombination mit Dexamethason.
Die höchste getestete Dosisgruppe (55 mg) überstieg die maximal verträgliche Dosis, da bei vier von sechs Patienten schwere Nebenwirkungen auftraten, einschließlich Neutropenie (niedrige weiße Blutkörperchen) und Thrombozytopenie (niedrige Thrombozytenzahl); daher wurde die geplante Höchstdosis von 70 mg nicht getestet.
Bei den Studienpatienten führte die Behandlung mit Melflufen und Dexamethason bei 76 % der Patienten zu einer Stabilisierung der Erkrankung.
Die mediane Zeit bis zur nächsten Behandlung – dem Beginn der Behandlung bis zur nächsten Behandlung (oder bis zum Tod des Patienten, je nachdem, was zuerst eintritt) – betrug 7,9 Monate. Die Patienten lebten im Median 20,7 Monate.
Klinische HORIZON-Studie
In der klinischen Phase-II-Studie HORIZON, die an 20 Standorten in den Vereinigten Staaten und in Europa stattfand, wurden Melflufen und Dexamethason an insgesamt 154 Patienten verabreicht, die durchschnittlich fünf vorherige Behandlungslinien erhalten hatten.
Alle Patienten waren zuvor mit einem immunmodulatorischen Medikament und einem Proteasom-Inhibitor behandelt worden und waren resistent gegen Pomalidomid und/oder Daratumumab.
Etwa drei von zehn Patienten (29 %) sprachen auf die Behandlung an, und die durchschnittliche Zeit bis zum Wiederauftreten des Myeloms betrug vier Monate. Diese Ergebnisse zeigten, dass Melflufen für Patienten von Vorteil sein kann, die zuvor mehrere Behandlungslinien erhalten haben.
Unerwünschte Ereignisse (UE) führten bei 27 % der Patienten zu einer Dosisreduktion von Melflufen und bei 61 % der Patienten zu einer Dosisverzögerung. Das häufigste UE, das zu einer Dosisreduktion führte, war Thrombozytopenie (niedrige Thrombozytenzahl), die bei 14 % der Patienten auftrat.
Bei insgesamt 49 % der Patienten traten schwerwiegende UE auf; am häufigsten wurden Lungenentzündung (9 %) und Neutropenie (5 %) berichtet. Zweite primäre Malignome traten bei fünf Patienten auf; von diesen hatten vier Malignome mit kutanen Manifestationen. Insgesamt starben 10 Patienten (6%) an behandlungsbedingten Nebenwirkungen.
Dosierung
Melflufen wird als intravenöse Infusion (in die Vene) verabreicht. In klinischen Studien war die Dosis:
- 40 mg Melflufen am ersten Tag jedes Behandlungszyklus
40 mg Dexamethason (reduzierte Dosis für Patienten ab 75 Jahren) an den Tagen 1, 8, 15 und 22 jedes 28-Tage-Zyklus
In einigen Studien wurde die Dosis bei denjenigen reduziert, bei denen eine Nebenwirkung auftrat.
Nebenwirkungen
Zu den am häufigsten beobachteten Nebenwirkungen von Melflufen gehören:
• Niedrige Anzahl von Blutkörperchen – Neutropenie und Thrombozytopenie
• Anämie
• Ermüdung
• Infektionen, einschließlich Lungenentzündung und Infektionen der oberen Atemwege
• Übelkeit und Durchfall
Da Melflufen ein relativ neues Medikament ist, können neue Nebenwirkungen auftreten, über die noch nicht berichtet wurde.
Risiken
Da die Forschung im Gange ist, ist es schwierig, die Risiken der Einnahme von Melflufen für RRMM einzuschätzen. Da Patienten, die für klinische Studien rekrutiert werden, häufig vorherige Behandlungen ausgeschöpft haben, besteht die Möglichkeit von Nebenwirkungen oder sogar Tod während und nach der Behandlung.
Infektionen sind aufgrund eines geschwächten Immunsystems eine der Hauptursachen für Morbidität und Mortalität bei Patienten mit RRMM. Es ist wichtig, sich regelmäßig auf Anzeichen einer Infektion zu überwachen und alle Bedenken so schnell wie möglich Ihrem Arzt zu melden.










Discussion about this post