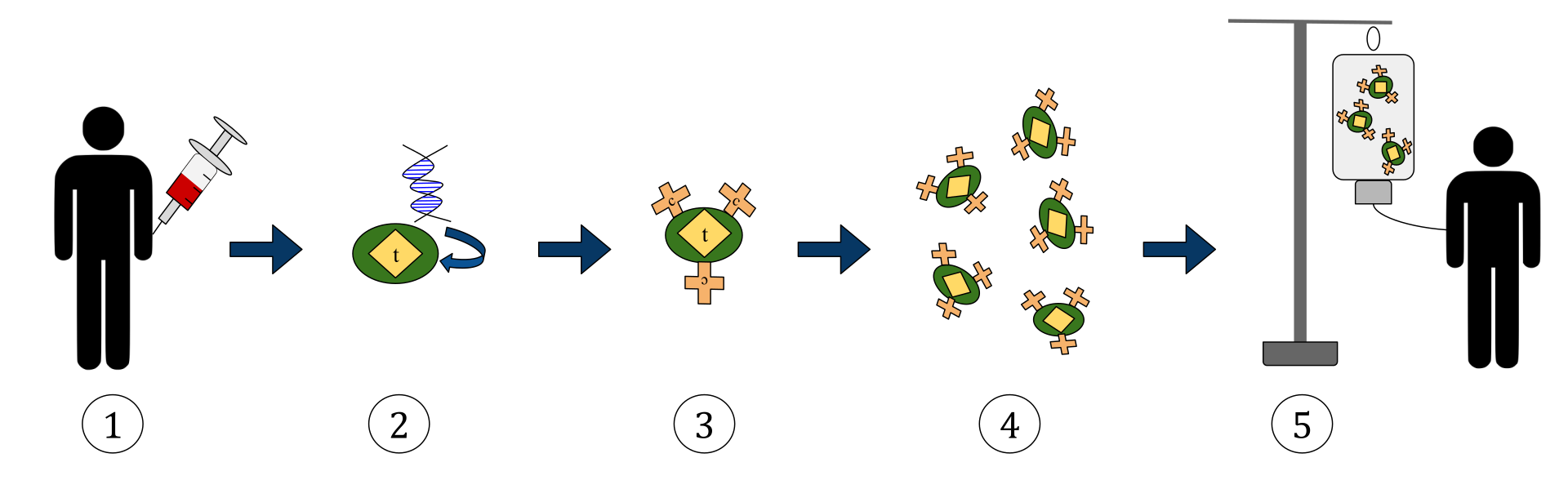
Das obige Diagramm zeigt den Prozess der T-Zelltherapie mit chimären Antigenrezeptoren (CAR). Dies ist eine Methode der Immuntherapie, die eine wachsende Praxis bei der Behandlung von Krebs ist. Das Endergebnis sollte eine Produktion von ausgestatteten T-Zellen sein, die die infizierten Krebszellen im Körper erkennen und bekämpfen können.
1. T-Zellen (dargestellt durch Objekte, die als „t“ gekennzeichnet sind) werden aus dem Blut des Patienten entfernt.
2. Dann wird in einer Laboreinstellung das Gen, das für die spezifischen Antigenrezeptoren kodiert, in die T-Zellen eingebaut.
3. So werden die CAR-Rezeptoren (markiert als c) auf der Oberfläche der Zellen erzeugt.
4. Die neu modifizierten T-Zellen werden dann weiter geerntet und im Labor gezüchtet.
5. Nach einer bestimmten Zeit werden die manipulierten T-Zellen wieder in den Patienten infundiert.
Chimäre Antigenrezeptor-T-Zellen (auch bekannt als CAR T-Zellen) sind T-Zellen, die gentechnisch verändert wurden, um einen künstlichen T-Zell-Rezeptor zur Verwendung in der Immuntherapie herzustellen.
Chimäre Antigenrezeptoren (Autos, auch bekannt als chimäre Immunrezeptoren, chimäre T-Zell-Rezeptoren, oder künstliche T-Zell-Rezeptoren) sind Rezeptorproteine, die entwickelt wurden, um T-Zellen die neue Fähigkeit zu geben, auf ein bestimmtes Protein abzuzielen. Die Rezeptoren sind chimär, weil sie sowohl Antigen-bindende als auch T-Zell-aktivierende Funktionen in einem einzigen Rezeptor kombinieren.
Die CAR-T-Zelltherapie verwendet T-Zellen, die mit CARs für die Krebstherapie entwickelt wurden. Die Prämisse der CAR-T-Immuntherapie besteht darin, T-Zellen so zu modifizieren, dass sie Krebszellen erkennen, um sie effektiver anzuvisieren und zu zerstören. Wissenschaftler ernten T-Zellen von Menschen, verändern sie genetisch und infundieren dann die resultierenden CAR-T-Zellen in Patienten, um ihre Tumore anzugreifen. CAR-T-Zellen können entweder von T-Zellen im eigenen Blut eines Patienten (autolog) oder von T-Zellen eines anderen gesunden Spenders (allogen) stammen. Sobald diese T-Zellen aus einer Person isoliert wurden, werden sie gentechnisch so verändert, dass sie ein spezifisches CAR exprimieren, das sie so programmiert, dass sie auf ein Antigen abzielen, das auf der Oberfläche von Tumoren vorhanden ist. Aus Sicherheitsgründen sind CAR-T-Zellen so konstruiert, dass sie spezifisch für ein Antigen sind, das auf einem Tumor exprimiert wird, der nicht auf gesunden Zellen exprimiert wird.
Nachdem CAR-T-Zellen in einen Patienten infundiert wurden, wirken sie als „lebendes Medikament“ gegen Krebszellen. Wenn sie mit ihrem Zielantigen auf einer Zelle in Kontakt kommen, binden CAR-T-Zellen daran und werden aktiviert, dann vermehren sie sich und werden zytotoxisch. CAR-T-Zellen zerstören Zellen durch verschiedene Mechanismen, einschließlich einer ausgedehnten stimulierten Zellproliferation, erhöhen den Grad ihrer Toxizität für andere lebende Zellen (Zytotoxizität) und verursachen die erhöhte Sekretion von Faktoren, die andere Zellen wie Zytokine, Interleukine und andere beeinflussen können Wachstumsfaktoren.
Produktion von CAR-T-Zellen

Der erste Schritt bei der Herstellung von CAR-T-Zellen ist die Isolierung von T-Zellen aus menschlichem Blut. CAR-T-Zellen können entweder aus dem eigenen Blut des Patienten hergestellt werden, das als autologe Behandlung bekannt ist, oder aus dem Blut eines gesunden Spenders, das als allogene Behandlung bekannt ist. Der Herstellungsprozess ist in beiden Fällen der gleiche; nur die Wahl des ursprünglichen Blutspenders ist unterschiedlich.
Zunächst werden Leukozyten unter Verwendung eines Blutzellseparators in einem als Leukozytenapherese bekannten Prozess isoliert. Periphere mononukleäre Blutzellen (PBMC) werden dann getrennt und gesammelt. Die Produkte der Leukozytenapherese werden dann in ein Zellverarbeitungszentrum überführt. Im Zellverarbeitungszentrum werden spezifische T-Zellen stimuliert, so dass sie sich aktiv vermehren und zu einer großen Anzahl expandieren. Um ihre Expansion voranzutreiben, werden T-Zellen typischerweise mit den Cytokin-Interleukin-2- (IL-2) und Anti-CD3-Antikörpern behandelt.
Die expandierten T-Zellen werden gereinigt und dann mit einem Gen, das das manipulierte CAR codiert, über einen retroviralen Vektor, typischerweise entweder ein integrierendes Gammaretrovirus (RV) oder einen lentiviralen (LV) Vektor, transduziert. Diese Vektoren sind in der heutigen Zeit aufgrund einer teilweisen Deletion der U3-Region sehr sicher. Das neue Gen-Editing-Tool CRISPR / Cas9 wurde kürzlich anstelle von retroviralen Vektoren verwendet, um das CAR-Gen in bestimmte Stellen im Genom zu integrieren.
Der Patient wird vor der Einführung der manipulierten CAR-T-Zellen einer Lymphodepletions-Chemotherapie unterzogen. Die Abnahme der Anzahl zirkulierender Leukozyten im Patienten erhöht die Anzahl der produzierten Zytokine und verringert den Wettbewerb um Ressourcen, was zur Förderung der Expansion der manipulierten CAR-T-Zellen beiträgt.
Klinische Anwendungen
Bis März 2019 wurden weltweit rund 364 klinische Studien mit CAR-T-Zellen durchgeführt. Die Mehrzahl dieser Studien zielt auf Blutkrebs ab: CAR-T-Therapien machen mehr als die Hälfte aller Studien zu hämatologischen Malignitäten aus. CD19 ist weiterhin das beliebteste Antigenziel, gefolgt von BCMA (üblicherweise im multiplen Myelom exprimiert). Im Jahr 2016 begannen Studien, die Lebensfähigkeit anderer Antigene wie CD20 zu untersuchen. Studien für solide Tumoren werden weniger von CAR-T dominiert, wobei etwa die Hälfte der auf Zelltherapie basierenden Studien andere Plattformen wie NK-Zellen einbezieht.
Krebs
T-Zellen werden gentechnisch so verändert, dass sie chimäre Antigenrezeptoren exprimieren, die spezifisch auf Antigene auf den Tumorzellen eines Patienten gerichtet sind, und dann in den Patienten infundiert werden, wo sie die Krebszellen angreifen und abtöten CAR-modifizierte T-Zellen können so konstruiert werden, dass sie auf praktisch jedes Tumor-assoziierte Antigen abzielen.
Die frühe CAR-T-Zellforschung hat sich auf Blutkrebs konzentriert. Die ersten zugelassenen Behandlungen verwenden CARs, die auf das Antigen CD19 abzielen, das bei von B-Zellen abgeleiteten Krebsarten wie akuter lymphoblastischer Leukämie (ALL) und diffusem großzelligem B-Zell-Lymphom (DLBCL) vorhanden ist. Es gibt auch Bemühungen, CARs zu entwickeln, die auf viele andere Blutkrebsantigene abzielen, einschließlich CD30 beim refraktären Hodgkin-Lymphom; CD33, CD123 und FLT3 bei akuter myeloischer Leukämie (AML); und BCMA beim multiplen Myelom.
Solide Tumoren haben ein schwierigeres Ziel dargestellt. Die Identifizierung guter Antigene war eine Herausforderung: Solche Antigene müssen in der Mehrzahl der Krebszellen stark exprimiert werden, in normalen Geweben jedoch weitgehend fehlen. CAR-T-Zellen werden auch nicht effizient in das Zentrum fester Tumormassen transportiert, und die feindliche Tumor-Mikroumgebung unterdrückt die T-Zell-Aktivität.
Autoimmunerkrankung
Während sich die meisten CAR-T-Zell-Studien auf die Schaffung einer CAR-T-Zelle konzentrieren, die eine bestimmte Zellpopulation ausrotten kann (z. B. CAR-T-Zellen, die auf Lymphomzellen abzielen), gibt es andere mögliche Anwendungen für diese Technologie. T-Zellen können auch Selbstantigene vor Autoimmunreaktionen schützen. Eine regulatorische T-Zelle, die mit einem CAR ausgestattet ist, könnte das Potenzial haben, einem bestimmten Antigen Toleranz zu verleihen, was bei Organtransplantationen oder rheumatischen Erkrankungen wie Lupus verwendet werden könnte.
Satefy
Es gibt schwerwiegende Nebenwirkungen, die sich aus der Einführung von CAR-T-Zellen in den Körper ergeben, einschließlich des Zytokinfreisetzungssyndroms und der neurologischen Toxizität. Da es sich um eine relativ neue Behandlung handelt, liegen nur wenige Daten zu den Langzeiteffekten der CAR-T-Zelltherapie vor. Es gibt immer noch Bedenken hinsichtlich des langfristigen Überlebens der Patientin sowie der Schwangerschaftskomplikationen bei weiblichen Patienten, die mit CAR-T-Zellen behandelt wurden. Anaphylaxie ist eine erwartete Nebenwirkung, da das CAR mit einem fremden monoklonalen Antikörper hergestellt wird und infolgedessen eine Immunantwort hervorruft.
On-Target / Off-Tumor-Erkennung tritt auf, wenn die CAR-T-Zelle das richtige Antigen erkennt, das Antigen jedoch auf gesundem, nicht pathogenem Gewebe exprimiert wird. Dies führt dazu, dass die CAR-T-Zellen Nicht-Tumorgewebe angreifen, wie beispielsweise gesunde B-Zellen, die CD19 exprimieren. Die Schwere dieser nachteiligen Wirkung kann von B-Zell-Aplasie, die mit unterstützenden Infusionen behandelt werden kann, bis zu extremer Toxizität, die zum Tod führt, variieren.
Es besteht auch die unwahrscheinliche Möglichkeit, dass die manipulierten CAR-T-Zellen selbst durch Insertionsmutagenese in Krebszellen umgewandelt werden, da der virale Vektor das CAR-Gen in einen Tumorsuppressor oder ein Onkogen im Genom der Wirts-T-Zelle einfügt. Einige retrovirale (RV) Vektoren tragen ein geringeres Risiko als lentivirale (LV) Vektoren. Beide können jedoch onkogen sein. Eine Genomsequenzierungsanalyse von CAR-Insertionsstellen in T-Zellen wurde zum besseren Verständnis der Funktion und Persistenz von CAR-T-Zellen in vivo etabliert.
Cytokin-Freisetzungssyndrom
Das häufigste Problem nach der Behandlung mit CAR-T-Zellen ist das Cytokin-Release-Syndrom (CRS), ein Zustand, bei dem das Immunsystem aktiviert wird und eine erhöhte Anzahl entzündlicher Cytokine freigesetzt wird. Die klinische Manifestation dieses Syndroms ähnelt einer Sepsis mit hohem Fieber, Müdigkeit, Myalgie, Übelkeit, Kapillarleckagen, Tachykardie und anderen Herzfunktionsstörungen, Leberversagen und Nierenfunktionsstörungen. CRS tritt bei fast allen Patienten auf, die mit CAR-T-Zelltherapie behandelt werden. Tatsächlich ist das Vorhandensein von CRS ein diagnostischer Marker, der anzeigt, dass die CAR-T-Zellen wie beabsichtigt arbeiten, um die Krebszellen abzutöten. Beachten Sie jedoch, dass ein höherer Schweregrad des CRS nicht mit einem erhöhten Ansprechen auf die Behandlung korreliert, sondern mit einer höheren Krankheitslast.
Immuneffektorzell-assoziierte Neurotoxizität
Neurologische Toxizität ist häufig auch mit der Behandlung von CAR-T-Zellen verbunden. Der zugrunde liegende Mechanismus ist kaum bekannt und kann mit CRS zusammenhängen oder nicht. Klinische Manifestationen sind Delirium, der teilweise Verlust der Fähigkeit, kohärent zu sprechen, während die Fähigkeit zur Interpretation der Sprache (expressive Aphasie) weiterhin besteht, verminderte Wachsamkeit (Obtundation) und Anfälle. Während einiger klinischer Studien sind Todesfälle aufgrund von Neurotoxizität aufgetreten. Die Haupttodesursache aufgrund von Neurotoxizität ist ein Hirnödem. In einer von Juno Therapeutics, Inc. durchgeführten Studie starben fünf an der Studie teilnehmende Patienten an den Folgen eines Hirnödems. Zwei der Patienten wurden nur mit Cyclophosphamid und die restlichen drei mit einer Kombination aus Cyclophosphamid und Fludarabin behandelt. In einer anderen klinischen Studie, die vom Fred Hutchinson Cancer Research Center gesponsert wurde, wurde 122 Tage nach der Verabreichung von CAR-T-Zellen ein Fall von irreversibler und tödlicher neurologischer Toxizität gemeldet.
.














Discussion about this post